Moderna a precizat că vaccinul său anti-COVID-19 în două doze a generat anticorpi neutralizanţi la copii, iar siguranţa serului este comparabilă cu cea constatată anterior în cazul studiilor clinice la adolescenţi şi adulţi.
Un comitet de specialişti din cadrul Agenţiei pentru alimente şi medicamente din Statele Unite (FDA) va lua marţi o decizie în ceea ce priveşte autorizarea serului produs de companiile concurente Pfizer şi BioNTech pentru utilizarea la copii cu vârste cuprinse între cinci şi 11 ani.
Vaccinul anti-COVID-19 produs de Moderna este autorizat pentru utilizare in regim de urgenţă în cazul adulţilor, iar recent a primit undă verde pentru administrarea unei a treia doze la anumite categorii de americani.
Cu toate acestea, FDA nu a autorizat încă vaccinul pentru a fi utilizat la adolescenţii cu vârste cuprinse între 12 şi 17 ani. Suedia a sistat utilizarea vaccinului Moderna pentru copiii din grupe mai mici de vârstă după ce au fost raportate cazuri de inflamaţie cardiacă la adulţi tineri.
Potrivit Moderna, cea mai mare parte a efectelor secundare din cadrul studiului clinic, care a inclus 4.753 de participanţi, au fost minore sau moderate din punctul de vedere al severităţii, a precizat compania. Cele mai frecvente efecte adverse raportate au fost oboseală, dureri de cap, febră şi durere la locul injectării, potrivit Agerpres.
Vaccinurile folosite în cadrul studiului au fost doze de 50 de micrograme, jumătate din concentraţia utilizată în vaccinurile administrate adulţilor. Doza de 50 de micrograme este de asemenea autorizată în cazul suprarapelului.








































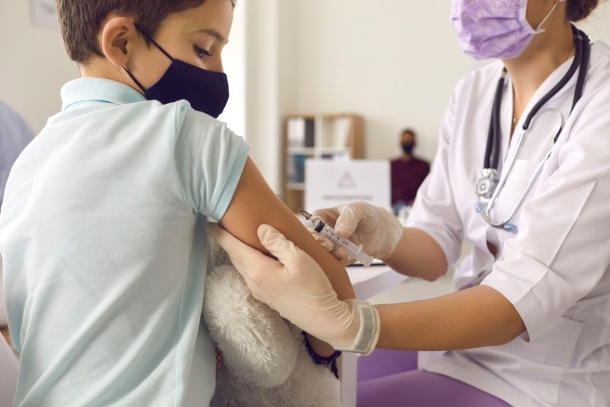
 De ce unii tineri fără comorbidităţi suferă forme de COVID-19 grave
De ce unii tineri fără comorbidităţi suferă forme de COVID-19 grave
 Vaccinul anti-COVID-19 dezvoltat de Pfizer are o eficienţă ridicată în rândul adolescenţilor
Vaccinul anti-COVID-19 dezvoltat de Pfizer are o eficienţă ridicată în rândul adolescenţilor